Regard moléculaire sur la transmission de la grippe aviaire à l’Homme
Des scientifiques de l’Institut de biologie structurale et du Laboratoire européen de biologie moléculaire de Grenoble publient dans la revue Nature Communications des résultats de recherche sur la transmission du virus de la grippe aviaire à l’Homme qui ouvrent de nouvelles voies thérapeutiques potentielles.
En recourant à une méthode RMN, les chercheurs de l’Institut de biologie structurale (IBS CNRS/CEA/UGA) et du Laboratoire européen de biologie moléculaire (EMBL) de Grenoble ont révélé les mécanismes moléculaires qui permettent au virus de la grippe aviaire de s'adapter de l'oiseau à l'Homme. En mettant à jour ces interactions entre la polymérase virale mutée et un facteur de transcription clé dans les cellules hôtes, ce nouveau regard permettra d'étudier le mécanisme de contagion inter-espèce de ces virus et donc d’ouvrir de nouvelles voies thérapeutiques potentielles.
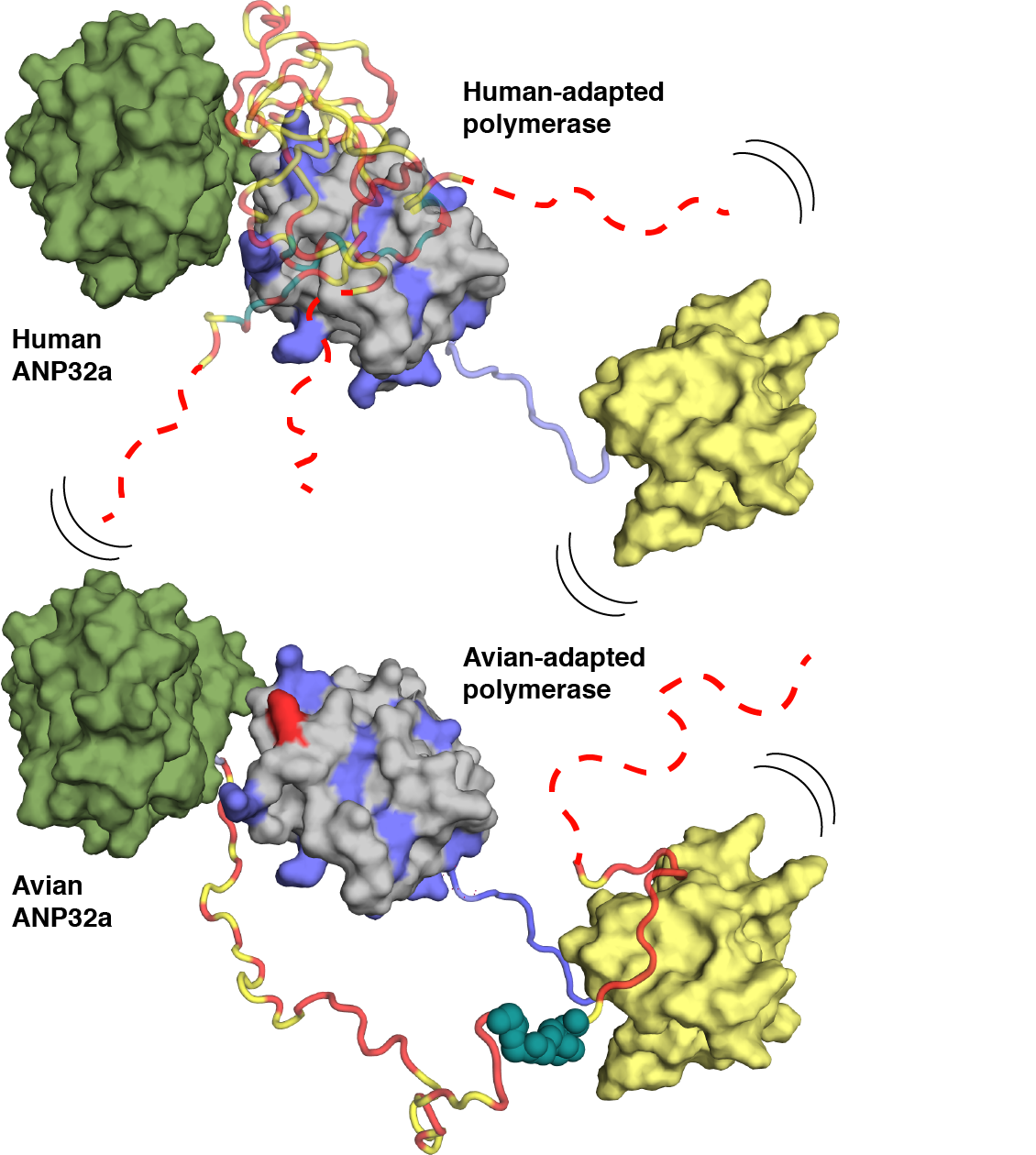
Chez l'oiseau, le virus de la grippe aviaire agit via l'interaction de sa polymérase avec un facteur de transcription clé : ANP32A. Sans que cette interaction soit bien connue, deux régions de ces molécules, très dynamiques, semblaient être particulièrement impliquées. Cette connaissance incomplète empêchait toutefois les chercheurs de comprendre comment certaines mutations de la polymérase virale lui permettait de s'adapter de l'oiseau à l'Homme, et acquérir ainsi une capacité de contagion inter-espèce. Ces régions moléculaires, très dynamiques (1), ne forment ni structures uniques, ni ne se cristallisent, compliquant leur étude.
Par la RMN, les chercheurs de l’Institut de biologie structurale de Grenoble sont parvenus à décrypter ces mécanismes : chez l'oiseau, la région dite "domaine 627-NLS" de la polymérase virale se fixe à une zone bien spécifique, impliquant un motif unique aviaire, du facteur de transcription ANP32A. Toutefois, ce motif n'existe pas dans la version humaine du facteur de transcription (2) - la polymérase virale n'a donc plus son port d'attache. Néanmoins des mutations changent la configuration de la polymérase : une mutation particulière de son domaine 627 permettent à la polymérase d'interagir avec toute la zone "modifiée" de la version humaine, sous la forme d'interactions certes moins spécifiques mais plus nombreuses - un peu à la manière du velcro. Le virus acquiert alors la possibilité d’infecter un nouvel hôte : l'Homme, pouvant ainsi se transmettre d'une espèce à une autre.
Cette étude fournit un cadre moléculaire pour comprendre les modes de liaison différentiels qui sous-tendent la restriction de la polymérase de la grippe par l'ANP32A chez certaines espèces et permettra d'identifier de nouvelles cibles pour l'inhibition de la grippe.
| Le virus de la grippe A (IAV) est annuellement responsable de 3 à 5 millions de cas, entraînant 250 à 500 000 décès. La plupart des souches de grippe évoluent exclusivement chez les oiseaux aquatiques, mais certaines souches aviaires hautement pathogènes (par exemple H5N1, H5N8, H7N9) peuvent infecter l'Homme avec des conséquences mortelles (jusqu'à 60 % de mortalité) et constituent une menace de pandémie pour l'humanité si elles développent une transmissibilité interhumaine. |
Notes
(1) Aussi appelée "intrinsèquement désordonnées", c’est-à-dire dépourvues de structure tridimensionnelle stable et fonctionnelles malgré tout dans cet état désordonné.
(2) La version humaine est déplétée de 33 acides aminés dans cette région du facteur de transcription.
En savoir +
Référence
Zarco AC, Kalayil S, Maurin D, Salvi N, Delaforge E, Milles S, Jensen MR, Hart DJ, Cusack S and Blackledge M. Molecular basis of host-adaptation interactions between influenza virus polymerase PB2 subunit and ANP32A. Nature Communications, 2020
Contact scientifique local
Institut de biologie structurale (IBS - CNRS / CEA / UGA)
Martin Blackledge, directeur adjoint de l’IBS, responsable du groupe de recherche Flexibilité et dynamique des protéines par RMN
martin.blackledge@ibs.fr